Thermodynamics Termodinamika
Cabang ilmu fisika yang mempelajari perilaku zat dibawah kontrol suhu
secara makroskopik
Thermodynamic System Sistem termodinamika atau sistem
atau system Sesuatu yang menjadi objek tinjauan
Surroundings Lingkungan
Segala sesuatu yang berada diluar sistem, yang berpengaruh secara
signifikan pada sistem
Boundary Batas
Permukaan nyata atau khayal yang memisahkan sistem dengan
lingkungan
Closed system Sistem tertutup
Sistem yang hanya mengizinkan interaksi usaha dan kalor, tetapi tidak
mengizinkan adanya interaksi massa
Open system Sistem terbuka
Sistem yang mengizinkan adanya interaksi usaha, kalor, dan massa
Isolated system Sistem terisolasi
Sistem yang tidak mengizinkan adanya interaksi kalor dengan
lingkungannya
Specific volume Volume jenis
Volume persatuan massa
Intensive properties Besaran intensif atau koordinat intensif
Besaran yang tidak bergantung pada ukuran sistem
Extensive properties Besaran ekstensif atau koordinat ekstensif
Besaran yang bergantung pada ukuran sistem
Blog ini dibuat oleh Innas Amalia Utami untuk memenuhi salah satu proyek mata kuliah Termodinamika dengan Dosen Pengampu Bapak Apit Fathurohman, S. Pd., M. Si
Selasa, 28 April 2015
perpindahan secara konduksi
Konduksi adalah proses perpindahan kalor tanpa disertai perpindahan partikel.
Konduksi adalah hantaran kalor yang tidak disertai dengan perpindahan
partikel perantaranya. Pada hantaran kalor ini yang berpindah hanyalah
energinya, tanpa melibatkan partikel perantaranya, seperti hantaran
kalor pada logam yang dipanaskan dari satu ujung ke ujung lainnya. Saat
ujung B dipanaskan, maka ujung A, lama kelamaan akan mengalami pemanasan
juga, hal tersebut dikarenakan energi kalor yang menggetarkan
molekul-molekul di ujung B turut menggetarkan molekul-molekul yang ada
disampingnya hingga mencapai titik A.
Sedang besar laju aliran kalor dengan konduksi dirumuskan,
H = laju aliran kalor (J/s atau watt)
Q = kalor yang dipindahkan (joule)
t = waktu (s)
k = konduktivitas termal zat (W/mK)
A = luas penampang melintang (m2)
∆t = perubahan suhu (°C atau K)
l = tebal penghantar (m)
Tabel konduktivitas termal zat
(W/mK)
| Bahan | k |
| Emas | 300 |
| Besi | 80 |
| Kaca | 0.9 |
| Kayu | 0.1 – 0.2 |
| Beton | 0.9 |
| Air | 0.6 |
| Udara | 0.024 |
| alumunium | 240 |
kerja dari batre
Korek api (kadang disebut juga geretan atau pematik) adalah sebuah alat untuk menyalakan api secara
terkendali. Korek api dijual bebas di toko-toko dalam bentuk paket
sekotak korek api. Sebatang korek api terdiri dari batang kayu yang salah satu ujungnya ditutupi dengan suatu bahan yang umumnya fosfor yang
akan menghasilkan nyala api karena gesekan ketika digesekkan terhadap
satu permukaan khusus walaupun ada tipe korek api yang dapat dinyalakan
pada sembarang permukaan kasar. Jenis korek api yang menggunakan cairan,
seperti naphtha atau butana, disebut korek api gas.

Korek api yang dinyalakan dengan digesek pertama kali ditemukan oleh kimiawan Inggris John Walker tahun 1827. Penemuan tersebut diawali oleh Robert Boyle tahun 1680-an dengan campuran fosfor dan belerang, tetapi usahanya pada waktu itu belum mencapai hasil yang memuaskan. Walker menemukan campuran antimon (III) sulfida, potasium klorat, natural gum, dan pati dapat dinyalakan dengan menggesekkannya pada permukaan kasar.
Pada
tahun 1800an, baja, batu geretan, dan sabuk/kawulmsih digunakan untuk
membuat api. Korek api pertama yang yg memakai fosfor dibuat pada tahun
1830an. Korek api disimpan pada sebuah kotak spesial karena dapat
terbakar pada permukaan apapun.Pada 1844, Profesor Gustaf Erik Pasch mengganti fosfor kuning yang beracun dengan fosfor merah yang tidak beracun. Dia juga memisahkan ramuan bahan kimia untuk ujung korek api dan meletakkan fosfor pada permukaan untuk digesek pada kotak luarnya. Korek api yang aman telah tercipta. Ini adalah sebuah hasil penemuan yang berarti dan penting, yang membuat Swedia terkenal di dunia. Sayang sekali, produksinya sungguh sulit dan mahal.
Pada tahun 1864, insinyur yang lebih tua 28 tahun, Alexander Lagerman mendesign korek api mesin otomatis yang pertama. Pada waktu itu, produksi yang menggunakan tangan atau secara manual berganti menjadi produksi massa, korek api yang aman dari korek api JONKOPING (swedia) diekspor keseluruh dunia dan menjadi terkenal di dunia.
Pada 1868, perusahaan korek api Vulcan AB ditemukan di Tidaholm, swedia. Sekarang, perusahaan Tidaholm, dimiliki oleh Swedish Macth, yang dianggap jalur produksinya memiliki teknologi paling yang paling berkembang dalam korek api di dunia. Pemikiran tentang Lingkungan adalah bagian yang sangat penting dalam proses menghasilkan produksi dan bahan kimia sudah diganti, kotak korek api sudah terbuat dari kertas yang didaur ulang.
Ada juga beberapa pendapat lain mengenai Korek api...
Sebatang korek api terdiri dari batang kayu yang salah satu ujungnya ditutupi dengan suatu bahan yang umumnya fosfor yang akan menghasilkan nyala api karena gesekan ketika digesekkan terhadap satu permukaan khusus.
Bangsa Tiongkok sejak 577 telah mengembangkan korek api sederhana yang terbuat dari batang kayu yang mengadung belerang. Korek api modern pertama ditemukan tahun 1805 oleh K. Chancel, asisten Profesor L. J. Thénard di Paris. Kepala korek api merupakan campuran potasium klorat, belerang, gula dan karet. Korek api ini dinyalakan dengan menyelupkannya ke dalam botol asbes yang berisi asam sulfat. Korek api ini tergolong mahal pada saat itu dan penggunaannya berbahaya sehingga tidak mendapatkan popularitas.
Korek api yang dinyalakan dengan digesek pertama kali ditemukan oleh kimiawan Inggris John Walker tahun 1827. Penemuan tersebut diawali oleh Robert Boyle tahun 1680-an dengan campuran fosfor dan belerang, tetapi usahanya pada waktu itu belum mencapai hasil yang memuaskan. Walker menemukan campuran antimon (III) sulfida, potasium klorat, natural gum, dan pati dapat dinyalakan dengan menggesekkannya pada permukaan kasar
balon udara
Sebelum kita mengetahui bagaimana cara kerja balon udara, ada baiknya kita ketahui terlebih dahulu bagian-bagian dari balon udara. Balon udara secara garis besarnya mempunyai tiga bagian utama yaitu envelope, burner, dan basket.
Envelope merupakan kantong yang terbuat dari bahan nilon berbentuk balon tempat udara dipanaskan. Karena nilon ini tidak tahan api, maka bagian bawah envelope dilapisi dengan bahan anti api (skirt). Envelope ini berisi udara/gas ringan (seperti gas hidrogen) yang berfungsi mengangkat balon udara dari landasannya.
Burner merupakan alat yang berfungsi untuk
memanaskan udara di dalam envelope. Burner di letakan di atas kepala
penumpang dekat ke mulut envelope. Burner ini mengatur tekanan dalam
kantung udara agar balon dapat terbang dengan ketinggian yang
diharapkan.
Basket atau keranjang merupakan tempat penumpang
mengendalikan balon udara atau penumpang yang menikmati penerbangan
balon udara. Basket dibuat dari bahan yang ringan dan lentur dan
terletak di bawah kantung udara.
Cara kerja balon udara sangat sederhana yaitu dengan cara memanaskan udara di dalam balon agar lebih panas dari udara di luarnya sehingga balon udara mengembang dan dapat naik (terbang). Udara yang lebih panas akan lebih ringan karena masa per unit volumenya lebih sedikit.
Untuk dapat terbang, udara di dalam envelope dipanaskan menggunakan
burner dengan temperatur sekitar 100 derajat Celcius. Udara panas ini
akan terperangkap di dalam envelope sehingga balon udara pun akan
mengembang dan bergerak naik di dorong oleh udara yang bertekanan lebih
kuat. Jika ingin mendarat, udara didinginkan dengan cara mengecilkan
burner. Udara yang mulai mendingin di dalam envelope membuat balon
bergerak turun.
Bagaimana caranya balon udara berpindah dari satu lokasi ke lokasi
lain? Jawabanya adalah dengan cara memanfaatkan hembusan angin untuk
bergerak secara horizontal. Arah tiupan angin berbeda pada setiap
ketinggian tertentu. Perbedaan arah tiupan angin inilah yang
dimanfaatkan oleh pengemudi balon udara untuk mengendalikan balon udara
dari satu lokasi ke lokasi yang diinginkan.
Balon udara mempunyai dua tipe yaitu:
1. Balon udara yang diisi dengan udara panas, yaitu balon udara yang
mempunyai pembakar yang berfungsi untuk memanaskan udara dalam balon
sehingga udara dalam balon menjadi lebih ringan dari udara luar
sekitarnya.
2. Balon udara yang diisi dengan gas yang memang ringan, yaitu balon udara yang diisi gas yang ringan seperti contohnya gas hydrogen. Namun kelemahan gas hidrogen ini adalah mudah terbakar. Jika ingin aman bisa menggunakan gas helium, namun sangat mahal.
2. Balon udara yang diisi dengan gas yang memang ringan, yaitu balon udara yang diisi gas yang ringan seperti contohnya gas hydrogen. Namun kelemahan gas hidrogen ini adalah mudah terbakar. Jika ingin aman bisa menggunakan gas helium, namun sangat mahal.
termometer digital
Termometer Digital
Dulu, termometer yang selalu menghiasi lemari obat biasanya termometer merkuri (air raksa). Namun sekarang termometer merkuri tidak lagi dianjurkan karena mudah pecah (terbuat dari kaca) dan merkurinya dapat menguap dan terhirup.
Ada beberapa jenis termometer. Dibawah ini adalah beberapa termometer yang juga dapat digunakan pada bayi. Sebelum memilihnya, sebaiknya pertimbangkan hal-hal berikut:
Termometer digital. Termometer yang satu inilah yang sering kita lihat dan gunakan. Memanfaatkan sensor panas elektrik untuk memeriksa suhu tubuh, termometer ini umum digunakan pada aksila (ketiak), oral (mulut) dan pada rektum (dubur).
Termometer telinga digital (membran timpani). Termometer ini memanfaatkan sinar inframerah untuk mengukur suhu tubuh melalui saluran telinga. Perlu diingat bahwa kotoran telinga atau saluran telinga yang melengkung dapat mengganggu keakuratannya.
Termometer empeng digital. Sesuai dengan namanya, bentuk termometer ini mirip dengan empeng bayi. Bayi hanya perlu menghisapnya untuk menggunakannya.
Termometer arteri temporalis. Termometer ini memanfaatkan scanner inframerah untuk mengukur suhu tubuh melalui arteri temporalis pada dahi.
Saran keamanan
Apapun jenis termometer yang Anda gunakan, bacalah dengan baik instruksi penggunaannya (biasanya disertakan dalam kemasan). Sebelum dan sesudah menggunakannya, bersihkan ujung termometer dengan alkohol atau sabun atau air hangat.
Jangan campur adukkan pemakaiannya. Misalnya satu termometer digunakan untuk mengukur ketiak, dubur dan mulut. Siapkan masing-masing satu termometer dan beri label pada setiap termometer agar tidak tertukar saat menggunakannya.
Untuk mencegah hal-hal yang tidak diinginkan dan agar termometer tetap di posisinya saat pengukuran, jangan meninggalkan anak bersama termometer. Temani ia hingga pengukuran selesai.
Pedoman penggunaan termometer sesuai usia
Termometer mana yang terbaik atau metode pemeriksaan mana yang terbaik, dalam beberapa kasus tergantung dari usia si anak. Berikut kami jelaskan:
Bayi di bawah 3 bulan. Gunakan termometer digital biasa dan ukur suhu pada bagian duburnya, ini lebih akurat daripada ketiak. Penelitian baru menunjukkan bahwa termometer arteri temporalis juga memberikan hasil yang cukup akurat pada bayi yang baru lahir.
Bayi 3 bulan sampai 4 tahun. Pemeriksan suhu di dubur tetap memberikan hasil yang terbaik untuk anak dibawah usia 3 tahun. Namun pada usia ini, pemeriksaan dengan termometer digital pada ketiak juga cukup akurat. Termometer arteri temporalis atau termometer empeng digital juga baik digunakan pada usia ini. Namun untuk menggunakan termometer telinga digital, sang anak harus berusia minimal 6 bulan. Jika Anda masih ragu dengan hasilnya, periksalah suhu duburnya.
Anak diatas 4 tahun. Anak-anak usia 4 tahun umumnya sudah bisa menggunakan termometer digital di mulut. Termometer digital biasa juga bisa digunakan pada ketiaknya. Termometer arteri temporalis atau termometer telinga digital juga baik digunakan pada usia ini.
Bagaimana cara mengukurnya?
Kami uraikan bagaimana cara mengukur suhu tubuh anak dengan termometer dan metode yang berbeda-beda:
Pada dubur. Aktifkan termometer digital biasa dan lumasi ujungnya dengan petroleum jelly. Baringkan terlentang bayi dan angkat pahanya, lalu masukkan termometer digital ke dalam dubur sedalam 1,3 cm sampai 2,5 cm. Tahan termometer hingga termometer sudah memberikan kode (biasanya nada) yang menandakan pengukuran sudah selesai. Cabut termometer dan lihat angkanya.
Pada mulut. Aktifkan termometer digital biasa. Tempatkan ujungnya di bawah lidah anak dan suruh dia menutup mulutnya. Jika termometer sudah memberi kode, cabut dan baca hasilnya. Jika anak baru saja selesai makan atau minum, tunggu setidaknya 30 menit sebelum melakukan pengukuran suhu di mulut. Jika terlihat anak Anda kesulitan menggunakan termometer di mulutnya (pernapasan terganggu), sebaiknya ganti dengan metode lain, misalnya pada ketiak.
Pada ketiak. Aktifkan termometer digital biasa. Pastikan Anda meletakkannya di bawah ketiak dan menyentuh kulit, bukan pakaian. Apit dengan erat hingga termometer memberikan kode. Lalu cabut dengan lembut dan baca hasilnya.
Pada telinga. Aktifkan termometer telinga digital. Perlahan tempatkan pada liang telinga anak Anda. Ikuti petunjuk yang disertakan pada kemasan termometer untuk memastikan Anda sudah tepat memasukkan termometer ke dalam liang telinga. Tahan sampai termometer memberikan kode bahwa pengukuran telah selesai. Cabut termometer dan baca hasilnya.
Pada arteri temporalis. Aktifkan termometer arteri temporalis. Sapukan termometer dengan lembut pada dahinya sampai termometer memberikan kode. Lalu angkat dan baca hasilnya.
Dulu, termometer yang selalu menghiasi lemari obat biasanya termometer merkuri (air raksa). Namun sekarang termometer merkuri tidak lagi dianjurkan karena mudah pecah (terbuat dari kaca) dan merkurinya dapat menguap dan terhirup.
Ada beberapa jenis termometer. Dibawah ini adalah beberapa termometer yang juga dapat digunakan pada bayi. Sebelum memilihnya, sebaiknya pertimbangkan hal-hal berikut:
Termometer digital. Termometer yang satu inilah yang sering kita lihat dan gunakan. Memanfaatkan sensor panas elektrik untuk memeriksa suhu tubuh, termometer ini umum digunakan pada aksila (ketiak), oral (mulut) dan pada rektum (dubur).
Termometer telinga digital (membran timpani). Termometer ini memanfaatkan sinar inframerah untuk mengukur suhu tubuh melalui saluran telinga. Perlu diingat bahwa kotoran telinga atau saluran telinga yang melengkung dapat mengganggu keakuratannya.
Termometer empeng digital. Sesuai dengan namanya, bentuk termometer ini mirip dengan empeng bayi. Bayi hanya perlu menghisapnya untuk menggunakannya.
Termometer arteri temporalis. Termometer ini memanfaatkan scanner inframerah untuk mengukur suhu tubuh melalui arteri temporalis pada dahi.
Saran keamanan
Apapun jenis termometer yang Anda gunakan, bacalah dengan baik instruksi penggunaannya (biasanya disertakan dalam kemasan). Sebelum dan sesudah menggunakannya, bersihkan ujung termometer dengan alkohol atau sabun atau air hangat.
Jangan campur adukkan pemakaiannya. Misalnya satu termometer digunakan untuk mengukur ketiak, dubur dan mulut. Siapkan masing-masing satu termometer dan beri label pada setiap termometer agar tidak tertukar saat menggunakannya.
Untuk mencegah hal-hal yang tidak diinginkan dan agar termometer tetap di posisinya saat pengukuran, jangan meninggalkan anak bersama termometer. Temani ia hingga pengukuran selesai.
Pedoman penggunaan termometer sesuai usia
Termometer mana yang terbaik atau metode pemeriksaan mana yang terbaik, dalam beberapa kasus tergantung dari usia si anak. Berikut kami jelaskan:
Bayi di bawah 3 bulan. Gunakan termometer digital biasa dan ukur suhu pada bagian duburnya, ini lebih akurat daripada ketiak. Penelitian baru menunjukkan bahwa termometer arteri temporalis juga memberikan hasil yang cukup akurat pada bayi yang baru lahir.
Bayi 3 bulan sampai 4 tahun. Pemeriksan suhu di dubur tetap memberikan hasil yang terbaik untuk anak dibawah usia 3 tahun. Namun pada usia ini, pemeriksaan dengan termometer digital pada ketiak juga cukup akurat. Termometer arteri temporalis atau termometer empeng digital juga baik digunakan pada usia ini. Namun untuk menggunakan termometer telinga digital, sang anak harus berusia minimal 6 bulan. Jika Anda masih ragu dengan hasilnya, periksalah suhu duburnya.
Anak diatas 4 tahun. Anak-anak usia 4 tahun umumnya sudah bisa menggunakan termometer digital di mulut. Termometer digital biasa juga bisa digunakan pada ketiaknya. Termometer arteri temporalis atau termometer telinga digital juga baik digunakan pada usia ini.
Bagaimana cara mengukurnya?
Kami uraikan bagaimana cara mengukur suhu tubuh anak dengan termometer dan metode yang berbeda-beda:
Pada dubur. Aktifkan termometer digital biasa dan lumasi ujungnya dengan petroleum jelly. Baringkan terlentang bayi dan angkat pahanya, lalu masukkan termometer digital ke dalam dubur sedalam 1,3 cm sampai 2,5 cm. Tahan termometer hingga termometer sudah memberikan kode (biasanya nada) yang menandakan pengukuran sudah selesai. Cabut termometer dan lihat angkanya.
Pada mulut. Aktifkan termometer digital biasa. Tempatkan ujungnya di bawah lidah anak dan suruh dia menutup mulutnya. Jika termometer sudah memberi kode, cabut dan baca hasilnya. Jika anak baru saja selesai makan atau minum, tunggu setidaknya 30 menit sebelum melakukan pengukuran suhu di mulut. Jika terlihat anak Anda kesulitan menggunakan termometer di mulutnya (pernapasan terganggu), sebaiknya ganti dengan metode lain, misalnya pada ketiak.
Pada ketiak. Aktifkan termometer digital biasa. Pastikan Anda meletakkannya di bawah ketiak dan menyentuh kulit, bukan pakaian. Apit dengan erat hingga termometer memberikan kode. Lalu cabut dengan lembut dan baca hasilnya.
Pada telinga. Aktifkan termometer telinga digital. Perlahan tempatkan pada liang telinga anak Anda. Ikuti petunjuk yang disertakan pada kemasan termometer untuk memastikan Anda sudah tepat memasukkan termometer ke dalam liang telinga. Tahan sampai termometer memberikan kode bahwa pengukuran telah selesai. Cabut termometer dan baca hasilnya.
Pada arteri temporalis. Aktifkan termometer arteri temporalis. Sapukan termometer dengan lembut pada dahinya sampai termometer memberikan kode. Lalu angkat dan baca hasilnya.
tekanan zat cair
TEKANAN ZAT CAIR
Air adalah zat cair, maka itu air dapat mengalir. Air mengalir dari tempat dengan energi potensial tinggi ke tempat dengan energi potensial rendah. Hal ini terjadi karena ada tekanan zat cair.
Hukum bejana berhubungan terjadi jika ke dalam bejana berhubungan diisikan satu jenis zat cair dalam keadaan seimbang, maka permukaan zat cair dalam bejana akan terletak pada bidang horisontal. Konsep bejana berhubungan yaitu apabila zat cair yang sejenis (satu jenis zat cair) dituangkan ke dalam suatu bejana, maka permukaan zat cair tersebut dalam bejana selalu mendatar dan sama tinggi. Prinsip ini diterapkan pada selang plastik sebagai alat sederhana yang memanfaatkan prinsip bejana berhubungan. Alat ini sering digunakan tukang bangunan untuk menentukan apakah tinggi dua titik yang berjauhan pada suatu tempat sama.
Apabila dua macam zat cair yang tidak sejenis dan tidak bercampur dituangkan ke dalam suatu bejana, maka permukaan zat cair yang tak sejenis tersebut tidak sama tinggi. Zat cair yang massa jenisnya lebih kecil, permukaannya lebih tinggi daripada zat cair yang massa jenisnya lebih besar. Oleh itu air, dapat mengalir.
Pada makalah ini akan dibahas sebagai berikut: Mengapa air dapat mengalir? Dapatkah air mengalir dari tempat rendah ke tempat yang tinggi? Bagaimana prinsip kerja pada aliran air PAM ke rumah-rumah? Apa contoh alat penggunaan hukum bejana berhubungan?
a. Mengapa air dapat mengalir?
Mengapa zat cair selalu dapat mengalir? Marilah kita tinjau lebih lanjut. Benda-benda apapun juga terdiri dari molekul-molekul, antara molekul-molekul yang terkandung didalam suatu benda terdapat celah-celah atau jarak. Tetapi bermacam-macam benda mempunyai jarak atau celah-celah antara molekul-molekul yang berlainan jenis pula. Pada zat padat seperti logam, kayu, karet atau batu jarak antara molekul-molekul sangat kecil satu sama lain tarik menarik dengan kuat nya, maka dari itu zat padat mempunyai bentuk dan volume yang tertentu. Hal ini berbeda dengan zat cair, jarak antara molekul-molekul zat cair agak besar, persatuan atau perpaduan antar molekul-molekul nya tidak begitu rapat dan sangat mudah terlepas dari ikatannya karena itu air dapat mengalir.
b. Dapatkah air mengalir dari tempat rendah ke tempat yang tinggi?
Pada prinsipnya air mengalir dari tempat yang tinggi ke tempat yang rendah. Air mengalir dari tempat yang tinggi ke tempat yang rendah, hal itu adalah sifat air. Hal ini bisa juga dipengaruhi oleh gravitasi bumi. Kalau tidak ada gravitasi air hanya mengambang saja. Selain itu, karena air mempunyai massa jenis lebih berat dari udara, jadi air selalu di bawah udara.
Air mengalir ke atas (lebih tinggi) bisa terjadi jika tekanan di bawah lebih tinggi dari di atas, misalnya pada sumur artesis. Hal ini terjadi karena adanya tekanan (power head) dari bawah menuju ke atas, maka terjadi selisih ketinggian air, di mana air di bagian yang ada power headnya lebih rendah dari yangg lain, sehingga air akan bergerak utk mencapai keseimbangan tinggi air (bejana berhubungan).
c. Bagaimana prinsip kerja pada aliran air PAM ke rumah-rumah?
Prinsip kerja pada aliran air PAM ke rumah-rumah melalui hukum pascal. Hukum pascal ialah jika suatu zat cair dikenakan tekanan, maka tekanan itu akan merambat ke segala arah dengan tidak bertambah atau berkurang kekuatannya.
Hukum Pascal menyatakan bahwa tekanan yang diberikan zat cair dalam ruang tertutup diteruskan ke segala arah dengan sama besar. Tekanan yang diberikan pada zat cair dalam ruang tertutup diteruskan ke segala arah dan sama besar. Air menyembur dari setiap lubang kantong plastik dengan jarak yang sama. Semakin kuat kantong plastik ditekan, semakin cepat semburan airnya begitu sebaliknya. Dengan demikian kita dapat menyimpulkan bahwa tekanan diteruskan ke segala arah dengan sama besar.
Jika penampang A1 diberi gaya F1 ke bawah, zat cair dalam penampang A1 mengalami tekanan P sebesar F1/A1. Kemudian tekanan akan diteruskan ke segala arah dengan sama besar, termasuk ke penampang A2. Seandainya gaya yang diberikan pada penampang A2 adalah F2 maka akan diperoleh persamaan seperti berikut :
F2 = P. A2 dimana P = F1/A1
Dengan demikian, sesuai dengan hukum Pascal diperoleh :
Air adalah zat cair, maka itu air dapat mengalir. Air mengalir dari tempat dengan energi potensial tinggi ke tempat dengan energi potensial rendah. Hal ini terjadi karena ada tekanan zat cair.
Hukum bejana berhubungan terjadi jika ke dalam bejana berhubungan diisikan satu jenis zat cair dalam keadaan seimbang, maka permukaan zat cair dalam bejana akan terletak pada bidang horisontal. Konsep bejana berhubungan yaitu apabila zat cair yang sejenis (satu jenis zat cair) dituangkan ke dalam suatu bejana, maka permukaan zat cair tersebut dalam bejana selalu mendatar dan sama tinggi. Prinsip ini diterapkan pada selang plastik sebagai alat sederhana yang memanfaatkan prinsip bejana berhubungan. Alat ini sering digunakan tukang bangunan untuk menentukan apakah tinggi dua titik yang berjauhan pada suatu tempat sama.
Apabila dua macam zat cair yang tidak sejenis dan tidak bercampur dituangkan ke dalam suatu bejana, maka permukaan zat cair yang tak sejenis tersebut tidak sama tinggi. Zat cair yang massa jenisnya lebih kecil, permukaannya lebih tinggi daripada zat cair yang massa jenisnya lebih besar. Oleh itu air, dapat mengalir.
Pada makalah ini akan dibahas sebagai berikut: Mengapa air dapat mengalir? Dapatkah air mengalir dari tempat rendah ke tempat yang tinggi? Bagaimana prinsip kerja pada aliran air PAM ke rumah-rumah? Apa contoh alat penggunaan hukum bejana berhubungan?
a. Mengapa air dapat mengalir?
Mengapa zat cair selalu dapat mengalir? Marilah kita tinjau lebih lanjut. Benda-benda apapun juga terdiri dari molekul-molekul, antara molekul-molekul yang terkandung didalam suatu benda terdapat celah-celah atau jarak. Tetapi bermacam-macam benda mempunyai jarak atau celah-celah antara molekul-molekul yang berlainan jenis pula. Pada zat padat seperti logam, kayu, karet atau batu jarak antara molekul-molekul sangat kecil satu sama lain tarik menarik dengan kuat nya, maka dari itu zat padat mempunyai bentuk dan volume yang tertentu. Hal ini berbeda dengan zat cair, jarak antara molekul-molekul zat cair agak besar, persatuan atau perpaduan antar molekul-molekul nya tidak begitu rapat dan sangat mudah terlepas dari ikatannya karena itu air dapat mengalir.
b. Dapatkah air mengalir dari tempat rendah ke tempat yang tinggi?
Pada prinsipnya air mengalir dari tempat yang tinggi ke tempat yang rendah. Air mengalir dari tempat yang tinggi ke tempat yang rendah, hal itu adalah sifat air. Hal ini bisa juga dipengaruhi oleh gravitasi bumi. Kalau tidak ada gravitasi air hanya mengambang saja. Selain itu, karena air mempunyai massa jenis lebih berat dari udara, jadi air selalu di bawah udara.
Air mengalir ke atas (lebih tinggi) bisa terjadi jika tekanan di bawah lebih tinggi dari di atas, misalnya pada sumur artesis. Hal ini terjadi karena adanya tekanan (power head) dari bawah menuju ke atas, maka terjadi selisih ketinggian air, di mana air di bagian yang ada power headnya lebih rendah dari yangg lain, sehingga air akan bergerak utk mencapai keseimbangan tinggi air (bejana berhubungan).
c. Bagaimana prinsip kerja pada aliran air PAM ke rumah-rumah?
Prinsip kerja pada aliran air PAM ke rumah-rumah melalui hukum pascal. Hukum pascal ialah jika suatu zat cair dikenakan tekanan, maka tekanan itu akan merambat ke segala arah dengan tidak bertambah atau berkurang kekuatannya.
Hukum Pascal menyatakan bahwa tekanan yang diberikan zat cair dalam ruang tertutup diteruskan ke segala arah dengan sama besar. Tekanan yang diberikan pada zat cair dalam ruang tertutup diteruskan ke segala arah dan sama besar. Air menyembur dari setiap lubang kantong plastik dengan jarak yang sama. Semakin kuat kantong plastik ditekan, semakin cepat semburan airnya begitu sebaliknya. Dengan demikian kita dapat menyimpulkan bahwa tekanan diteruskan ke segala arah dengan sama besar.
Jika penampang A1 diberi gaya F1 ke bawah, zat cair dalam penampang A1 mengalami tekanan P sebesar F1/A1. Kemudian tekanan akan diteruskan ke segala arah dengan sama besar, termasuk ke penampang A2. Seandainya gaya yang diberikan pada penampang A2 adalah F2 maka akan diperoleh persamaan seperti berikut :
F2 = P. A2 dimana P = F1/A1
Dengan demikian, sesuai dengan hukum Pascal diperoleh :
Beberapa alat yang bekerja berdasarkan hukum Pascal adalah dongkrak hidrolik, rem hidrolik dan alat pengangkat mobil.
Teknologi yang membantu sistem kerja aliran air PAM ke rumah-rumah diberi nama microhydrolic. Prinsip kerjanya, air kotor yang disedot dari sungai mengalir akan diteruskan ke bak penampungan pertama yang terdiri atas 10 bak. Di bak-bak ini akan dilangsungkan pemisahan air yang bisa digunakan dan air yang tidak bisa digunakan. Lalu dilakukan predesinfektan. Kemudian air dimasukkan ke bakflocculator untuk diolah kembali. Setelah ada peningkatan kualitas, air kembali dialirkan ke bak sedimentasi. Di bak sedimentasi akan terjadi pemisahan antara air dan endapan-endapan tak terpakai yang selanjutnya akan dibuang. Sedangkan air bersih dialirkan ke rumah-rumah. Untuk dapat mengalirkan air ke rumah-rumah diperlukan tekanan yang cukup memadai.
d. Apa contoh alat penggunaan hukum bejana berhubungan?
Zat cair menekan ke segala arah. Zat cair akan memberi tekanan ke semua arah yang ada dengan besar yang sama, hal ini terjadi karena menganut hukum bejana berhubungan. Contohnya: apabila ember yang berisi air kita beri lubang di banyak tempat maka terlihat bahwa air mengucur dari semua lubang yang ada.
Contoh kerja alat penggunaan hukum bejana berhubungan dapat dilihat pada gambar di bawah ini. Pada gambar dapat dilihat bahwa lubang bejana yang paling bawah menyemburkan air paling jauh. Hal ini menunjukkan bahwa pada bagian yang paling dalam tekanannya paling besar.
Selain itu, kita juga menemukan bahwa air dan minyak menghasilkan zat cair yang berbeda jauhnya. Dengan demikian, massa jenis zat cair berpengaruh juga terhadap besar kecilnya tekanan. Persamaannya dapat ditulis sebagai berikut:
kulkas

Gambar 1. Kulkas
Tahukah anda mengapa pada saat tangan tersentuh alkohol,
maka alcohol akan segera menguap dan tangan anda terasa dingin?
Menguapnya alkohol disebabkan titik uap alkohol lebih rendah dari air,
sehingga alkohol lebih mudah menguap. Pada saat alkohol menguap, maka
alkohol membutuhkan sejumlah kalor yang diambil dari tangan anda,
akibatnya suhu di sekitar kulit tangan anda akan mengalami penurunan.
Hal inilah yang menghasilkan sensasi dingin di tangan anda.
Kita perhatikan kasus lain:
Di siang bolong anda berada di tengah lapang di bawah
terik matahari, tiba-tiba anda mendapatkan tetes-tetes air dari selang
yang disemprotkan teman anda ke arah udara. Maka anda pun akan merasa
dingin yang menyegarkan, walaupun suhu di sekitar anda tetap tinggi. Hal
tersebut diakibatkan oleh menguapnya tetes-tetes air tersebut yang
sempat mengenai kulit Anda. Sekali lagi menguapnya air-air tersebut di
kulit anda akan mengambil panas di kulit anda yang pada akhirnya
menghasilkan sensasi dingin di kulit anda. Jika hal tersebut dilakukan
terus menerus dalam waktu satu jam lebih, Anda tidak lagi sekedar
merasa dingin, tapi suhu tubuh anda akan turun dan anda dapat sakit.
Prinsip di atas menjadi dasar cara kerja kulkas
Uap cairan tertentu yang disebut refrigerant
disemprotkan terus menerus ke dalam ruangan kulkas yang akan mengambil
kalor dari makanan-makanan di kulkas. Namun berbeda dengan alkohol atau
tetes-tetes air, titik uap refrigerant jauh lebih rendah,
yaitu sekitar -27° F, sehingga kalor yang diambil tidak digunakan untuk
mengubahnya menjadi uap, tetapi sekedar menaikkan suhu refrigerant.
Jenis-jenis Kulkas
Jenis Non Frezer

Gambar 2. Jenis kulkas Non Freezer
Lemari Es (kulkas) di rumah kita digolongkan nonfrezer
apabila bagian di dalam lemari Es tidak hanya
evaporator (bagian pembeku). Pada kulkas satu pintu evaporatornya
terletak di bagian atas dan ukurannya tidak lebih 1/3 ukuran total
kulkasnya. Pada kulkas dua pintu dan seterusnya evaporator tersendiri
dan ukurannya lebih besar dibandingkan evaporator kulkas satu pintu.
Temperatur dingin pada rak-rak dibawah evaporator,
sebenarnya berasal dari hembusan udara dingin dari evaporator. Bagian
rak ini biasa digunakan untuk menyimpan makanan dan minuman.
Jenis Frezer

Gambar 3. Kulkas jenis Freezer
Lemari es freezer dapat membekukan atau
menjadikan sesuatu menjadi Es di setiap bagiannya. Biasanya , lemari es
jenis ini digunakan untuk kegiatan wirausaha , seperti penjual es batu
atau es lilin. Tidak seperti kulkas biasanya kulkas freezer memiliki evaporator di setiap raknya. Jadi kulkas freezer mampu membekukan lebih banyak dibandingkan lemari es nonfreezer.
Jenis Door Glass Refrigerator

Gambar 4. Kulkas jenis Door Glass Refrigerator
Kulkas pintu kaca termasuk jenis kulkas nonfreezer.
Kulkas jenis ini digunakan khusus untuk menyimpan aneka minuman kaleng
dan botol. Dengan pintu terbuat dari kaca, memungkinkan minuman yang
berada di dalam terlihat dari luar. Temperatur yang dihasilkan oleh
kulkas pintu kaca berkisar antara 10°-16° celcius. Kulkas ini tidak
membekukan minuman yang ada di dalamnya, tetapi hanya mendinginkannya
atau menyegarkannya.
proses kerja mesin turbojet
Mesin turbojet menjadi salah satu jenis mesin penggerak pesawat terbang.
Mesin penggerak pesawat terbang yang juga banyak digunakan pada saat
ini selain turbojet yaituturboprop danturbofan.
Mesin turbojet sangat umum digunakan pada pesawat-pesawat tempur yang
membutuhkan kecepatan tinggi. Dan sekalipun mesin ini tidak lazim
digunakan pada kendaraan darat, namun kendaraan untuk pemecahan rekor
kecepatan darat menggunakan mesin ini.
Mesin turbojet merupakan penerapan dari siklus termodinamika Brayton (baca artikel siklus brayton berikut).
Siklus Brayton terbagi kedalam empat tahapan proses yakni proses
kompresi isentropik, proses pembakaran isobarik, proses ekspansi
isentropik, serta proses pembuangan panas. Keempat tahapan proses inilah
yang menjadi prinsip dasar dari mesin turbojet.
Prinsip kerja mesin turbojet tidak dapat terlepas dengan
komponen-komponen kerjanya. Komponen utama dari mesin turbojet yaitu
kompresor, ruang bakar (combustion chamber),
turbin, dan nozzle. Tiga tahapan awal dari siklus brayton di atas
terjadi pada komponen-komponen mesin turbojet tersebut. Sedangkan proses
siklus brayton yang terakhir yakni proses pembuangan panas, terjadi di
udara atmosfer.
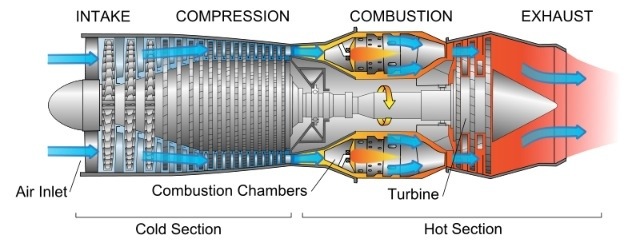
Skema Mesin Turbojet
(Sumber)
(Sumber)
Mesin turbojet menggunakan udara atmosfer sebagai fluida kerja. Udara
masuk ke dalam sistem turbojet melalui sisi inlet kompresor. Saat
melewati kompresor, udara dikompresi oleh beberapa tingkatan sudu
kompresor yang tersusun secara aksial. Pada ujung akhir kompresor,
penampang casingberbentuk
difuser untuk menambah tekanan keluaran kompresor. Umumnya, tekanan
udara keluaran kompresor turbojet mencapai rasio 15:1. Selain itu, ada
sebagian udara bertekanan yang tidak diteruskan masuk ke ruang bakar.
Sebagian kecil udara bertekanan tersebut diekstraksi untuk berbagai
kebutuhan seperti pendinginan stator turbin, air conditioning, dan untuk sistem pencegah terbentuknya es di sisi inlet turbin.
Selanjutnya, udara terkompresi keluaran kompresor masuk ke ruang bakar atau combustor. Bahan bakar (avtur contohnya) diinjeksikan ke dalam ruang bakar ini. Sistemcombustor memiliki
desain khusus sehingga aliran udara bertekanan akan mengkabutkan bahan
bakar. Campuran bahan bakar dan udara dipicu untuk terbakar di dalam
ruang bakar ini. Proses pembakaran yang terjadi seolah-olah menghasilkan
efek ledakan yang membuat udara bertekanan memuai dengan sangat cepat.
Pemuaian udara yang terjadi membuat udara panas hasil pembakaran
berekspansi secara bebas ke arah turbin.

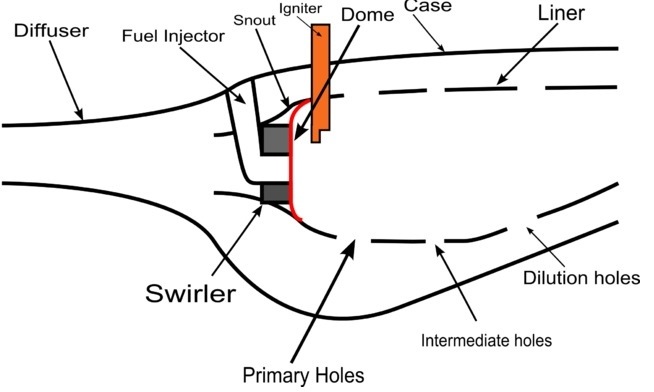
Potongan Penampang Combustor dan Bagian-bagiannya
Udara panas hasil pembakaran di combustor akan
menuju sisi turbin. Turbin tersusun atas beberapa tingkatan sudu rotor
dan stator. Sudu-sudu turbin berfungsi sebagai nozzle-nozzle kecil yang
akan mengkonversikan energi panas di dalam udara pembakaran menjadi
energi kinetik. Sudu pada sisi rotor turbin yang dapat berputar
mengkonversikan energi kinetik ini menjadi energi mekanis putaran poros
turbojet. Karena turbin dan kompresor berada pada satu poros, maka
energi putar poros digunakan untuk memutar kompresor turbojet.
Berbeda dengan mesin turbin gas pada PLTG yang keseluruhan energi panas
udara hasil pembakaran dikonversikan menjadi putaran poros, pada mesin
turbojet sebagian besar energi panas justru tidak digunakan untuk
memutar turbin. Sebagian besar energi panas ini dikonversikan menjadi
daya dorong (thrust)
mesin yang dibutuhkan untuk penggerak pesawat terbang. Untuk
mengkonversi energi panas udara menjadi daya dorong, pada sisi keluaran
turbin mesin jet terdapat nozzle besar dengan penampang selebar mesin
jet itu sendiri. Nozzle besar ini berfungsi untuk merubah energi panas
udara menjadi kecepatan tinggi sebagai komponen daya dorong.
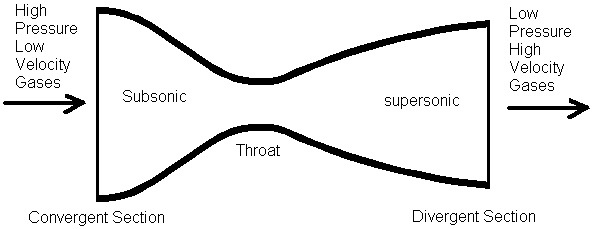
Prinsip Nozzel Konvergen-Divergen Digunakan Pada ExhaustMesin Turbojet
(Sumber)
(Sumber)
Sebuah pesawat jet yang mampu mencapai kecepatan supersonik (melebihi kecepatan suara) pasti exhaust mesin
jetnya menggunakan nozzle konvergen-divergen. Nozzle konvergen-divergen
adalah sebuah pipa yang mengalami pencekikan aliran di
tengah-tengahnya, menghasilkan bentuk seperti jam pasir yang tidak
simetris antara sisi inlet dan outlet nozzle. Nozzle ini berfungsi untuk
mengakselerasi gas panas dengan tekanan tinggi sehingga mencapai
kecepatan supersonik. Bentuk nozzle yang sedemikian rupa membuat energi
panas yang mendorong aliran udara terkonversi secara maksimal menjadi
energi kinetik.
Penampang cekik dari nozzle pada mesin jet bertujuan untuk menciptakan
restriksi aliran udara panas sehingga tekanan udara meningkat, yang
biasanya bahkan mendekati chockingatau
berhentinya aliran udara. Lalu aliran udara panas yang tercekik ini
secara tiba-tiba diekspansikan hingga mencapai atau paling tidak
mendekati tekanan atmosfer. Ekspansi ini diakibatkan oleh bentuk nozzle
divergen setelah bagian cekiknya. Ekspansi cepat hingga mencapai tekanan
atmosfer inilah yang mengkonversikan energi panas udara menjadi daya
dorong pesawat.


Exhaust Nozzle Dengan Sistem Vektor Fleksibel
(Sumber)
(Sumber)
Dapat disimpulkan bahwa energi untuk mendorong pesawat berasal dari
temperatur dan tekanan udara panas hasil pembakaran di dalam combustor.
Udara hasil pembakaran inilah yang mengakselerasi pesawat jet menjadi
kecepatan supersonik. Akselerasi yang diberikan oleh udara panas
tersebut tergantung oleh beberapa kondisi berikut:
- Tekanan dan temperatur udara panas di titik masuk nozzle.
- Tekanan ambien keluaran nozzle.
- Efisiensi dari proses ekspansi. Efisiensi ini meliputi kerugian atas adanya gesekan, atau adanya kemungkinan kebocoran pada nozzle.
Gaya Dorong Mesin Turbojet
Berikut adalah rumus perhitungan gaya dorong netto mesin turbojet:
Dimana:
 = laju massa aliran udara di dalam mesin jet.
= laju massa aliran udara di dalam mesin jet.
 = laju massa aliran bahan bakar di dalam mesin jet.
= laju massa aliran bahan bakar di dalam mesin jet.
 = kecepatan keluaran fluida jet.
= kecepatan keluaran fluida jet.
 = kecepatan udara masuk ke inlet mesin jet.
= kecepatan udara masuk ke inlet mesin jet.
defenisi kalor laten
Sebagaimana telah kita lihat dalam bagian sebelumnya, suatu zat dapat
mengalami perubahan suhu ketika energi ditransfer antara zat tersebut
dan sekitarnya. Dalam beberapa situasi, transfer energi tidak
mengakibatkan perubahan suhu. Ini adalah kasus kapanpun karakteristik
fisik dari perubahan substansi dari satu bentuk ke bentuk lainnya,
perubahan tersebut sering disebut sebagai perubahan fase. Dua perubahan
fasa umum adalah dari padat menjadi cair (mencair) dan dari cair ke gas
(mendidih), yang lain adalah perubahan dalam struktur kristal yang
solid. Semua perubahan fase tersebut melibatkan perubahan energi
internal sistem tetapi tidak ada perubahan suhu. Kenaikan energi
internal dalam mendidih, misalnya, diwakili oleh pemecahan ikatan antara
molekul dalam keadaan cair, ini melanggar ikatan memungkinkan molekul
untuk bergerak jauh terpisah dalam bentuk gas, dengan peningkatan yang
sesuai dalam energi potensial antarmolekul.
Seperti yang Anda duga, zat yang berbeda merespon secara berbeda
terhadap penambahan atau pengurangan energi mereka ketika berubah fase
karena pengaturan molekul internal mereka bervariasi. Juga, jumlah
energi yang ditransfer selama fase perubahan tergantung pada jumlah zat
yang terlibat. (Dibutuhkan sedikit energi untuk melelehkan es batu
daripada yang dilakukannya untuk mencairkan danau beku.) Ketika membahas
dua tahap material, kita akan menggunakan istilah bahan fase lebih
tinggi yang berarti materi yang ada pada suhu yang lebih tinggi. Jadi,
misalnya, jika kita membahas air dan es, air adalah bahan yang lebih
tinggi fasenya, sedangkan uap adalah bahan yang lebih tinggi fasenya
dalam membahas uap dan air. Pertimbangkan sebuah sistem yang mengandung
zat dalam dua tahap dalam kesetimbangan seperti air dan es. Jumlah awal
bahan fase tinggi, air, dalam sistem adalah mi. Sekarang bayangkan bahwa
energi Q memasuki sistem. Akibatnya, jumlah akhir air mf karena
mencairnya sebagian es. Oleh karena itu, jumlah es yang mencair, sama
dengan jumlah air yang baru, adalah ∆m = mf - mi. Kita mendefinisikan
kalor laten untuk perubahan fasa sebagai:
L ≡ Q/∆m
(20.6)
Parameter ini disebut kalor laten (harfiah, kalot "tersembunyi") karena
ini penambahkan atau pengurangan energi yang tidak mengakibatkan
perubahan suhu. Nilai L untuk bahan tergantung pada sifat dari perubahan
fasa serta sifat-sifat zat. Jika seluruh jumlah bahan berfase lebih
rendah mengalami perubahan fase, perubahan massa ∆m dari bahan berfase
lebih tinggi adalah sama dengan massa awal bahan berfase lebih rendah.
Sebagai contoh, jika es batu bermassa m di piring mencair sepenuhnya,
perubahan massa air mf - 0 = m, yang merupakan massa air baru dan juga
sama dengan massa awal es batu.

Dari definisi kalor laten, dan lagi memilih kalor sebagai mekanisme
transfer energi kita, energi yang dibutuhkan untuk mengubah fase zat
murni
Q = L ∆m
di mana ∆m adalah perubahan massa bahan yang fasenya lebih tinggi.
Kalor laten fusi Lf adalah istilah yang digunakan ketika perubahan fase
dari padat menjadi cair (untuk memadukan cara "menggabungkan dengan
peleburan"), dan kalor laten penguapan Lv adalah istilah yang digunakan
ketika perubahan fasa dari cair ke gas (cairan "menguap"). Kalor laten
berbagai zat bervariasi seperti data yang ditunjukkan pada Tabel 20.2.
Ketika energi memasuki sistem, menyebabkan pencairan atau penguapan,
jumlah bahan dengan fase lebih tinggi meningkat, sehingga ∆m positif dan
Q adalah positif, konsisten dengan konvensi tanda kita. Ketika energi
diekstrak dari sistem, menyebabkan pembekuan atau kondensasi, jumlah
materi dengan fase lebih tinggi menurun, sehingga ∆m adalah negatif dan Q
adalah negatif, sekali lagi konsisten dengan konvensi tanda kita. Perlu
diingat bahwa ∆m dalam Persamaan 20.7 selalu mengacu pada materi dengan
fase yang lebih tinggi.
Untuk memahami peran dari kalor laten dalam perubahan fase,
mempertimbangkan energi yang dibutuhkan untuk mengubah sebuah kubus es
1,0 g pada suhu -30,0 0C menjadi uap pada suhu 120,0 0C. Gambar 20.3
menunjukkan hasil eksperimen yang diperoleh ketika energi secara
bertahap ditambahkan ke es. Hasil disajikan sebagai grafik suhu sistem
es batu dibandingkan energi yang ditambahkan ke sistem. Mari kita
periksa setiap bagian dari kurva merah-coklat, yang dibagi menjadi
beberapa bagian A sampai E.

 Bagian A. Pada bagian kurva ini, perubahan suhu es dari -30,0 0C sampai
0,00C. Persamaan 20.4 menunjukkan bahwa suhu berubah secara linear
dengan energi yang ditambahkan, sehingga hasil eksperimen adalah garis
lurus pada grafik. Karenakalor jenis es 2090 J/kg∙0C, kita dapat
menghitung jumlah energi yang ditambahkan dengan menggunakan Persamaan
20.4:
Q = mici ∆T = (1,0 x 10-3 kg) (2090 J/kg∙0C) (30,0 0C) = 62,7 J
Bagian B. Ketika suhu es mencapai 0,0 0C, campuran es-air tetap pada
suhu ini-bahkan meskipun energi yang ditambahkan- sampai semua es
mencair. Energi yang dibutuhkan untuk mencairkan 1,00 g es pada suhu 0,0
0C, dari Persamaan 20.7,
Q = Lf ∆mw = Lfmi = (3,33 x 105 J/kg) (1.00 x 10-3 kg) = 333 J
Pada titik ini, kita telah pindah ke 396 J (=62,7 J + 333 J) tanda pada
sumbu energi pada Gambar 20.3.
Bagian C. Antara 0,0 0C dan 100,0 0C, ada yang mengejutkan terjadi.
Tidak ada perubahan fase terjadi, dan sehingga semua energi yang
ditambahkan ke dalam air digunakan untuk meningkatkan suhu. Jumlah
energi yang diperlukan untuk meningkatkan suhu dari 0,0 0C sampai 100,0
0C:
Q = mwcw ∆T = (1,00 x 10-3 kg) (4,19 x 103 J/kg∙0C) (100,0 0C) = 419 J
Bagian D. Pada 100,0 0C, perubahan fasa yang lain terjadi karena
perubahan air dari air pada 100,0 0C menjadi uap pada 100,0 0C. Serupa
dengan campuran air es di bagian B, campuran air-uap tetap pada 100,0
0C-meskipun energi yang ditambahkan-sampai semua cairan telah dikonversi
menjadi uap. Energi yang dibutuhkan untuk mengkonversi 1,00 g air
menjadi uap pada 100,0 0C:
Q = Lv ∆ms = Lvmw = (2,26 x 106 J/kg) (1,00 x 10-3 kg) = 2,26 x 103 J
Bagian E. Pada bagian kurva ini, seperti di bagian A dan C, tidak ada
perubahan fase terjadi, karena itu, semua energi yang ditambahkan
digunakan untuk meningkatkan suhu uap. Energi yang harus ditambahkan
untuk menaikkan suhu uap dari 100,0 0C sampai 120,0 0C:
Q = mscs ∆T = (1,00 x 10-3 kg) (2,01 x 103 J/kg∙0C) (20,0 0C) = 40,2 J
Jumlah total energi yang harus ditambahkan untuk mengubah 1 g es pada
suhu -30,0 0C menjadi uap pada suhu 120,0 0C adalah jumlah dari hasil
dari lima bagian kurva, yaitu 3,11 x 103 J. Sebaliknya, untuk
mendinginkan 1 g uap pada 120,0 0C menjadi es pada suhu -30,0 0C, kita
harus menghilangkan 3,11 x 103 J energi.
Perhatikan pada Gambar 20.3 jumlah yang relatif besar dari energi yang
ditransfer ke dalam air untuk diuapkan menjadi uap. Bayangkan
membalikkan proses ini, dengan sejumlah besar energi yang ditransfer
dari uap mengembun menjadi air. Itu sebabnya luka bakar pada kulit Anda
dari uap pada suhu 100 0C jauh lebih merusak daripada paparan kulit Anda
ke air pada suhu 100 0C. Sejumlah energi yang sangat besar memasuki
kulit Anda dari uap, dan uap tetap pada 100 0C untuk waktu yang lama
sementara itu mengembun. Sebaliknya, bila kulit Anda mengalami kontak
dengan air pada suhu 100 0C, air segera mulai turun suhunya sebagai
transfer energi dari air ke kulit Anda.
Jika air cair dibiarkan diam dalam wadah yang sangat bersih, adalah
mungkin bagi air untuk turun suhunya di bawah 0 0C tanpa membeku menjadi
es. Fenomena ini, yang disebut supercooling (pendinginan), muncul
karena air memerlukan gangguan semacam molekul untuk bergerak terpisah
dan mulai membentuk jadi besar, struktur es terbuka yang membuat
kepadatan es lebih rendah dari air seperti yang dibahas dalam Bagian
19.4. Jika air super dingin terganggu, ia tiba-tiba membeku. Sistem
menetes ke konfigurasi energi yang lebih rendah dari molekul terikat
dari struktur es, dan energi yang dilepaskan menaikkan suhu kembali ke 0
0C.
Tangan komersial penghangat terdiri dari natrium asetat cair dalam
kantong plastik tertutup. Solusi dalam kantong dalam keadaan stabil
superdingin. Ketika disk dalam kantong diklik oleh jari-jari Anda,
cairan membeku dan suhu meningkat, seperti air super dingin yang
disebutkan. Dalam kasus ini, bagaimanapun, titik beku cairan lebih
tinggi dari suhu tubuh, sehingga kantong terasa hangat saat disentuh.
Untuk menggunakan kembali tangan hangat, kantong harus direbus sampai
padat mencair. Kemudian, karena cools, melewati bawah titik beku ke
keadaan super dingin.
Hal ini juga memungkinkan untuk membuat superheating. Misalnya, air
bersih dalam cangkir sangat bersih ditempatkan dalam oven microwave
kadang-kadang dapat kenaikan suhu melebihi 100 0C tanpa mendidih karena
pembentukan gelembung uap dalam air membutuhkan goresan dalam cangkir
atau beberapa jenis kotoran dalam air untuk melayani sebagai situs
nukleasi. Ketika cangkir dipindahkan dari oven microwave, air
superheated bisa menjadi ledakan seperti gelembung yang terbentuk segera
dan air panas dipaksa ke atas dari cangkir (Serway,2010:572-575).
Bagian A. Pada bagian kurva ini, perubahan suhu es dari -30,0 0C sampai
0,00C. Persamaan 20.4 menunjukkan bahwa suhu berubah secara linear
dengan energi yang ditambahkan, sehingga hasil eksperimen adalah garis
lurus pada grafik. Karenakalor jenis es 2090 J/kg∙0C, kita dapat
menghitung jumlah energi yang ditambahkan dengan menggunakan Persamaan
20.4:
Q = mici ∆T = (1,0 x 10-3 kg) (2090 J/kg∙0C) (30,0 0C) = 62,7 J
Bagian B. Ketika suhu es mencapai 0,0 0C, campuran es-air tetap pada
suhu ini-bahkan meskipun energi yang ditambahkan- sampai semua es
mencair. Energi yang dibutuhkan untuk mencairkan 1,00 g es pada suhu 0,0
0C, dari Persamaan 20.7,
Q = Lf ∆mw = Lfmi = (3,33 x 105 J/kg) (1.00 x 10-3 kg) = 333 J
Pada titik ini, kita telah pindah ke 396 J (=62,7 J + 333 J) tanda pada
sumbu energi pada Gambar 20.3.
Bagian C. Antara 0,0 0C dan 100,0 0C, ada yang mengejutkan terjadi.
Tidak ada perubahan fase terjadi, dan sehingga semua energi yang
ditambahkan ke dalam air digunakan untuk meningkatkan suhu. Jumlah
energi yang diperlukan untuk meningkatkan suhu dari 0,0 0C sampai 100,0
0C:
Q = mwcw ∆T = (1,00 x 10-3 kg) (4,19 x 103 J/kg∙0C) (100,0 0C) = 419 J
Bagian D. Pada 100,0 0C, perubahan fasa yang lain terjadi karena
perubahan air dari air pada 100,0 0C menjadi uap pada 100,0 0C. Serupa
dengan campuran air es di bagian B, campuran air-uap tetap pada 100,0
0C-meskipun energi yang ditambahkan-sampai semua cairan telah dikonversi
menjadi uap. Energi yang dibutuhkan untuk mengkonversi 1,00 g air
menjadi uap pada 100,0 0C:
Q = Lv ∆ms = Lvmw = (2,26 x 106 J/kg) (1,00 x 10-3 kg) = 2,26 x 103 J
Bagian E. Pada bagian kurva ini, seperti di bagian A dan C, tidak ada
perubahan fase terjadi, karena itu, semua energi yang ditambahkan
digunakan untuk meningkatkan suhu uap. Energi yang harus ditambahkan
untuk menaikkan suhu uap dari 100,0 0C sampai 120,0 0C:
Q = mscs ∆T = (1,00 x 10-3 kg) (2,01 x 103 J/kg∙0C) (20,0 0C) = 40,2 J
Jumlah total energi yang harus ditambahkan untuk mengubah 1 g es pada
suhu -30,0 0C menjadi uap pada suhu 120,0 0C adalah jumlah dari hasil
dari lima bagian kurva, yaitu 3,11 x 103 J. Sebaliknya, untuk
mendinginkan 1 g uap pada 120,0 0C menjadi es pada suhu -30,0 0C, kita
harus menghilangkan 3,11 x 103 J energi.
Perhatikan pada Gambar 20.3 jumlah yang relatif besar dari energi yang
ditransfer ke dalam air untuk diuapkan menjadi uap. Bayangkan
membalikkan proses ini, dengan sejumlah besar energi yang ditransfer
dari uap mengembun menjadi air. Itu sebabnya luka bakar pada kulit Anda
dari uap pada suhu 100 0C jauh lebih merusak daripada paparan kulit Anda
ke air pada suhu 100 0C. Sejumlah energi yang sangat besar memasuki
kulit Anda dari uap, dan uap tetap pada 100 0C untuk waktu yang lama
sementara itu mengembun. Sebaliknya, bila kulit Anda mengalami kontak
dengan air pada suhu 100 0C, air segera mulai turun suhunya sebagai
transfer energi dari air ke kulit Anda.
Jika air cair dibiarkan diam dalam wadah yang sangat bersih, adalah
mungkin bagi air untuk turun suhunya di bawah 0 0C tanpa membeku menjadi
es. Fenomena ini, yang disebut supercooling (pendinginan), muncul
karena air memerlukan gangguan semacam molekul untuk bergerak terpisah
dan mulai membentuk jadi besar, struktur es terbuka yang membuat
kepadatan es lebih rendah dari air seperti yang dibahas dalam Bagian
19.4. Jika air super dingin terganggu, ia tiba-tiba membeku. Sistem
menetes ke konfigurasi energi yang lebih rendah dari molekul terikat
dari struktur es, dan energi yang dilepaskan menaikkan suhu kembali ke 0
0C.
Tangan komersial penghangat terdiri dari natrium asetat cair dalam
kantong plastik tertutup. Solusi dalam kantong dalam keadaan stabil
superdingin. Ketika disk dalam kantong diklik oleh jari-jari Anda,
cairan membeku dan suhu meningkat, seperti air super dingin yang
disebutkan. Dalam kasus ini, bagaimanapun, titik beku cairan lebih
tinggi dari suhu tubuh, sehingga kantong terasa hangat saat disentuh.
Untuk menggunakan kembali tangan hangat, kantong harus direbus sampai
padat mencair. Kemudian, karena cools, melewati bawah titik beku ke
keadaan super dingin.
Hal ini juga memungkinkan untuk membuat superheating. Misalnya, air
bersih dalam cangkir sangat bersih ditempatkan dalam oven microwave
kadang-kadang dapat kenaikan suhu melebihi 100 0C tanpa mendidih karena
pembentukan gelembung uap dalam air membutuhkan goresan dalam cangkir
atau beberapa jenis kotoran dalam air untuk melayani sebagai situs
nukleasi. Ketika cangkir dipindahkan dari oven microwave, air
superheated bisa menjadi ledakan seperti gelembung yang terbentuk segera
dan air panas dipaksa ke atas dari cangkir (Serway,2010:572-575).
karakteristikk beberapa bahan bakar
Bensin
Solar
| Struktur kimia | : C10 s/d C20 |
| Cetane number | : 40 s/d 55 |
| Angka oktan | : 8 s/d 15 |
| Massa jenis | : 0,832 kg/l |
| Sumber | : minyak bumi |
| Kandungan energi | : 35.677 – 36.235 kJoule per liter |
| Fase | : cair |
| Emisi | : menghasilkan gas buang berbahaya (ex.: sulfur, NOx, karbon monoksida) dan partikel padat. |
BioSolar
| Struktur kimia | : Metil ester dari C16 s/d C18 |
| Cetane number | : 46 s/d 60 |
| Angka oktan | : ~25 |
| Massa jenis | : 0,88 kg/l |
| Sumber | : minyak kedelai, bekas minyak goreng, lemak hewani |
| Kandungan energi | : 32.611 – 33.447 kJoule per liter |
| Fase | : cair |
| Emisi | : menghasilkan gas buang yang bahayanya lebih rendah daripada solar biasa. |
Compressed Natural Gas
| Struktur kimia | : CH4 |
| Angka oktan | : 120 |
| Massa jenis | : 0,7 kg/m3 |
| Sumber | : bawah tanah |
| Kandungan energi | : 9.198 – 10.592 kJoule per liter pada tekanan 3000psi |
| Fase | : gas bertekanan |
| Emisi | : ramah lingkungan, CO2 rendah |
Etanol
| Struktur kimia | : CH3CH2OH |
| Angka oktan | : 100 |
| Massa jenis | : 789 kg/m3 |
| Sumber | : jagung, padi, sampah agrikultur. |
| Kandungan energi | : 22.298 kJoule per liter |
| Fase | : cair |
| Emisi | : ramah lingkungan |
Hidrogen
| Struktur kimia | : H2 |
| Angka oktan | : 120 |
| Massa jenis | : 70,99 kg/m3 (fase cair); 0,0899 kg/m3 (fase gas temperatur & tekanan ruang) |
| Sumber | : bawah tanah. |
| Kandungan energi | : 20.487 kJoule per liter |
| Fase | : cair atau gas |
| Emisi | : ramah lingkungan |
Liquified Petroleum Gas
| Struktur kimia | : C3H8 |
| Angka oktan | : 104 |
| Massa jenis | : 582,37 kg/m3 (fase cair); 18,357 kg/m3 (fase gas) |
| Sumber | : pengolahan petroleum atau gas alam |
| Kandungan energi | : 23.413 kJoule per liter |
| Fase | : cair atau gas |
| Emisi | : ramah lingkungan |
Metanol
| Struktur kimia | : CH3OH |
| Angka oktan | : 100 |
| Massa jenis | : 791,8 kg/m3 |
| Sumber | : gas alam, batubara, atau biomass dari kayu. |
| Kandungan energi | : 15.609 – 18.396 kJoule per liter |
| Fase | : cair |
| Emisi | : ramah lingkungan |
Langganan:
Komentar (Atom)





